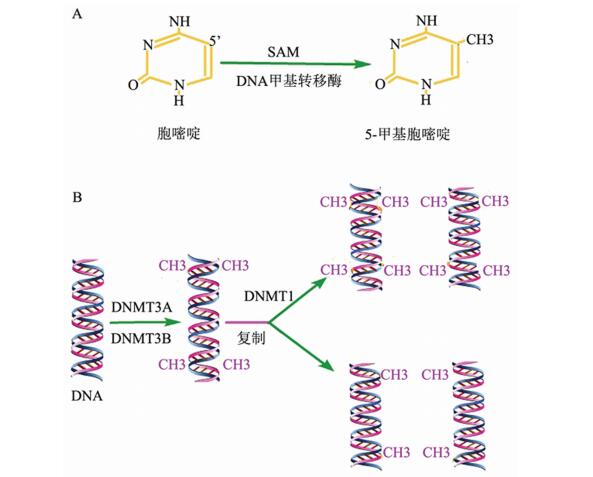
DNA修复基因的启动子甲基化06-甲基鸟嘌呤DNA甲基成立
尽管采用手术联合以替莫唑胺为基础的放化疗进行多模式治疗,但胶质母细胞瘤的预后仍然很差。根据加拿大国家癌症研究所临床试验组的欧洲癌症研究和治疗组织进行的一项 III 期试验,2005 年引入了放射治疗与伴随和维持 TMZ 作为护理标准的概念。同时,建立了具有 06-甲基鸟嘌呤 DNA 甲基化的 DNA 修复基因的启动子甲基化,其中 TMZ 作为化疗受益的预测生物标志物。在一项研究中,前 TMZ 时代基于人群的总生存期为 4.9 个月和 8.1 个月。2005 年引入 TMZ 后,美国研究在 2005-2008 年的 OS 为 9.7 个月,在苏黎世的 OS 为 11 个月,瑞士。这至少部分可以解释为在复发时增加使用各种虽然效果不大的治疗方案。TMZ 或亚硝基脲和贝伐单抗的烷基化化疗是复发性胶质母细胞瘤最常用的药物。该试验在首次复发时比较了两种不同剂量密集的 TMZ 方案,表明 TMZ 的益处可能仅限于具有 MGMT 启动子甲基化的肿瘤患者。
贝伐单抗于 2009 年在美国和其他几个国家有条件地获得批准,基于在复发性胶质母细胞瘤患者的两项 II 期临床研究中令人鼓舞的放射反应率。3 期试验将患者随机分配到贝伐单抗或洛莫司汀单药治疗或两者的组合。两个单药治疗组的中位 OS 为 8 个月,而联合治疗组为 12 个月。然而,在随后的临床试验中,与洛莫司汀单药治疗相比,该组合的 OS 益处尚未得到证实。然而,鉴于剂量密集的 TMZ 在具有启动子未甲基化肿瘤的 MGMT 患者中表现不佳,因此假设贝伐单抗可能是这组复发性胶质母细胞瘤患者的首选。
可获得来自接受烷化剂 TMZ 或基于亚硝基脲的方案作为单一药物或与其他化疗药物联合使用或首次使用贝伐单抗治疗胶质母细胞瘤复发的患者的临床数据,以及初始肿瘤的启动子甲基化状态以及 MGMT 信息。首次复发时接受贝伐单抗和伊立替康联合治疗的患者被纳入,但排除了接受贝伐单抗联合任何其他联合治疗的患者,包括接受烷化剂和贝伐单抗联合治疗的患者。患者队列由在德国神经胶质瘤网络中心接受治疗的患者组成,这是一个涉及德国八个临床中心的前瞻性非干预性队列,在苏黎世大学医院进行回顾性分析和治疗,瑞士。在苏黎世大学医院接受治疗的 41 名患者的子集的数据已包含在以前的出版物中。这项研究得到了德国德国神经胶质瘤网络负责审查委员会和瑞士苏黎世大学医院参与中心的批准。没有关于肿瘤进展的中央放射学审查。根据各自的进展时间,标准或 RANO 标准在现场局部应用。根据当地标准,使用甲基化特异性 PCR 或焦磷酸测序评估启动子的 MGMT 甲基化状态。使用当地标准检测异柠檬酸脱氢酶 1 或 IDH2 突变状态;它可用于 243 名患者:通过免疫组织化学评估 74 个肿瘤,通过 IDH1/2 测序评估 154 个肿瘤,甲基化分析为3个肿瘤。该方法无法在 12 名患者的临床图表审查中指定。
初始胶质母细胞瘤诊断后的无进展生存期从初始手术到肿瘤进展计算,OS 从初始手术到死亡或最后一次随访计算。PFS-2 是针对第二次复发接受全身治疗的患者亚组计算的,定义为从第一次复发全身治疗的第一天到第二次复发开始治疗干预之日的时间段。复发后的存活率是从全身性疾病的复发到死亡的第一天或最后一次接触的日期计算的。从第二次复发到死亡或最后一次接受药物治疗的日期,在接受全身治疗的第二次复发患者亚组中计算了 PRS-2。在最后一次随访时对患者进行检查。患者年龄数据由中位数和范围描述。对于分类数据,给出了绝对频率和相对频率。通过比较A组患者特征与B组x2检验、精确检验和检验。通过对数秩检验分析生存数据并呈现为-曲线。Cox 回归分析用于评估 PRS-1 与根据年龄、一线治疗、初次手术程度和 MGMT 状态调整的化疗的关联。所有分析均由版本 25 执行。Cox 回归分析用于评估 PRS-1 与根据年龄、一线治疗、初次手术程度和 MGMT 状态调整的化疗的关联。所有分析均由版本 25 执行。Cox 回归分析用于评估 PRS-1 与根据年龄、一线治疗、初次手术程度和 MGMT 状态调整的化疗的关联。所有分析均由版本 25 执行。
344例烷化剂化疗或贝伐单抗由海外医疗服务机构确定。总结了人口统计学和临床特征的细节。年龄、性别、一线治疗的差异和首次复发时的手术范围在各组之间得到了很好的平衡,而初次手术的范围、PFS-1、体能状态、MGMT 启动子甲基化状态和 IDH 突变状态。A组138例,B组20例MGMT肿瘤启动子甲基化。A 组 192 名患者可进行 IDH 检测:其中 23 名患者进行了 IDH 检测。在 B 组中,51 名患者可进行 IDH 检测,均为同源野生型。为了解释患者特征的这种不平衡,
整个队列的 344 名患者中有 307 人死亡。存活患者的中位随访时间为 22.1 个月。接受烷化剂化疗的患者的 PRS-1 时间长于接受贝伐单抗的患者。已知 IDH 状态的患者亚组和排除 IDH 突变肿瘤的患者亚组相似。PRS-1复发的手术没有预后。注意到两个队列之间预后因素的差异,可能与医生选择的第一次抢救治疗有关。与首例复发病例相比,贝伐单抗不再将 PFS-1 置于烷化剂上,并且这些人群的初步诊断显示 OS。中位 PFS-1 为 8.7 个月,PRS-1 为 11.1 个月,6. 首次复发患者接受烷化化疗1个月贝伐单抗治疗耐药患者分别为7.1)和7.4。对于已知 IDH 疾病且排除 IDH 突变肿瘤的患者亚组,中位 PFS-1 为 8.7 个月,中位 PRS-1 为 11.1 个月6.9 个月和 7.1 个月。对使用烷化剂治疗的患者进行亚组分析,以了解使用 TMZ 或亚硝基脲分层时 PFS-1 或 OS 的差异。首次复发的 TMZ 患者的 PFS-1 和 OS 都比亚硝基脲更长。对于已知 IDH 状态且不包括 IDH 突变肿瘤的患者亚组,
接下来按 MGMT 启动子甲基化状态对患者队列进行分层。在未甲基化启动子甲基化肿瘤患者中,接受烷化剂化疗的患者首次复发时 PRS-1 的 MGMT 较长。对于接受贝伐单抗的患者,MGMT 启动子甲基化状态与 PRS-1 相同。对于同时具有甲基化和未甲基化 MGMT 启动子的患者,接受烷基化化疗的两组 PRS-1 都比贝伐单抗组长。在已知 IDH 状态和排除 IDH 突变肿瘤的患者亚组中,接受烷基化化疗的甲基化患者与未甲基化患者相比,只有 MGMT 启动子较差的趋势。为了比较接受烷基化化疗和贝伐单抗的患者,较长的 PRS-1 仅在 MGMT 启动子甲基化肿瘤患者中观察到,但在 MGMT 启动子未甲基化肿瘤患者之间没有差异。如上所述,还调查了这些患者组的整体疾病轨迹。在甲基化和非甲基化 MGMT 启动子的情况下,与贝伐单抗相比,在使用烷化剂的患者中,PFS-1 和 OS 更长。对于排除 IDH 突变肿瘤的患者亚组,有和没有 MGMT 启动子甲基化的 PFS-1 没有显着差异,而有和没有 MGMT 的 OS 在接受烷化药物的患者中与接受贝伐单抗的患者相比更长。还调查了这些患者组的整体疾病轨迹。在甲基化和非甲基化 MGMT 启动子的情况下,与贝伐单抗相比,在使用烷化剂的患者中,PFS-1 和 OS 更长。对于排除 IDH 突变肿瘤的患者亚组,有和没有 MGMT 启动子甲基化的 PFS-1 没有显着差异,而有和没有 MGMT 的 OS 在接受烷化药物的患者中与接受贝伐单抗的患者相比更长。还调查了这些患者组的整体疾病轨迹。在甲基化和非甲基化 MGMT 启动子的情况下,与贝伐单抗相比,在使用烷化剂的患者中,PFS-1 和 OS 更长。对于排除 IDH 突变肿瘤的患者亚组,有和没有 MGMT 启动子甲基化的 PFS-1 没有显着差异,而有和没有 MGMT 的 OS 在接受烷化药物的患者中与接受贝伐单抗的患者相比更长。
在排除 IDH 突变肿瘤患者后,当肿瘤在已知 IDH 状态和结果的亚组中含有甲基化 MGMT 启动子时,未使用过烷化剂的患者具有更长的 PFS-1 和 OS。用烷化剂治疗的患者组中的中位 PFS-1 为具有 5.0 个月 MGMT 启动子甲基化肿瘤和 6.5 个月 MGMT 启动子未甲基化甲基化肿瘤的患者,以及按甲基化和未甲基化分层的患者接受贝伐单抗的 MGMT 启动子状态分别需要 8.7 个月和 5.6 个月。在用烷化剂治疗的组中,MGMT 启动子甲基化的中位 PRS-1 为 12.2 个月,MGMT 启动子未甲基化的胶质母细胞瘤患者为 8.7 个月。接受贝伐单抗 8.2 个月和 < @7.3 个月。显示了按 MGMT 状态分层的中位 PFS-1 和中位 PRS-1 用于不包括 IDH 突变肿瘤的亚组。

PRS 的差异也可能取决于随后的抢救治疗。表格显示了第二次或多次复发的不同补救疗法的详细信息。首次复发时接受贝伐单抗的烷基化化疗患者的 PRS-1 比接受贝伐单抗的患者更长,并且首次复发时烷基化化疗挽救治疗的任何进一步进展 p=0.002。对于已知 IDH 状态且不包括 IDH 突变的肿瘤亚组,整个患者队列(不包括 IDH 突变肿瘤亚组)的中位 PFS-1 和中位 PRS-1 总结了结果参数的 95% 置信区间。对于那些因第二次复发而接受进一步全身性挽救治疗的患者,评估从第一次复发开始全身性治疗到任何第二次复发开始挽救性治疗的中位时间,并且从第二次复发的全身治疗开始存活到死亡或最后一次暴露日期。贝伐单抗组在第一次复发时接受任何其他全身挽救治疗的患者的统计分析被省略,但由于患者数量少,在第二次复发时没有烷化药物 IDH 突变的肿瘤。与先接受贝伐单抗的患者相比,先接受烷基化化疗然后接受含贝伐单抗方案的患者的 PFS-2 没有差异,但 PRS-1 和 PRS-2 更长。之后是烷化剂。PFS-2 较短,而第二次或更晚使用烷化剂和贝伐单抗抢救治疗的患者的 PRS-1 和 PRS-2 与任何其他抢救治疗的患者相当,但没有贝伐单抗没有差异。对于已知 IDH 状态和 IDH 突变肿瘤的排除亚组,在比较接受烷基化的患者时,PFS-2 和更长的 PRS-1 和 PRS-2 没有差异。化疗后采用含贝伐单抗的方案,贝伐单抗后采用烷化剂。在该亚群中,PFS-2、PRS-1 和 PRS-2 在先接受烷化剂然后接受贝伐单抗治疗的患者与任何其他补救治疗相比没有差异。
进行多变量 Cox 回归分析以考虑在首次复发时使用烷化剂治疗的患者与含贝伐单抗的方案治疗 PRS-1 的潜在预后因素的差异。从一个模型开始,该模型包括所有年龄段的可用文献、MGMT 启动子甲基化、一线治疗和初次手术切除的范围。与贝伐单抗相比,在首次复发时接受烷化剂治疗的患者中,年龄和 MGMT 启动子甲基化与预后相关。KPS 作为新诊断的胶质母细胞瘤的已知预后因素被从该分析中省略,因为没有预后作用,并且在评估 TMZ 在复发性胶质母细胞瘤和复发中的指导试验中关于 KPS 的数据仅部分适用于患者。接下来比较 PRS-1 的 Cox 回归模型在首次复发时接受贝伐单抗治疗并进行烷化化疗的患者与首次接受贝伐单抗治疗的患者在首次复发和任何进一步复发的患者之间进行比较。首先用烷化剂治疗,在进一步复发时未接受贝伐单抗治疗的患者先用贝伐单抗治疗,然后不使用烷化剂。在该模型中,与贝伐单抗初治患者和随后的烷化剂相比,首次复发后接受贝伐单抗治疗的患者的 PRS-1 差异不显着。此外,该模型表明,与既往使用贝伐单抗后未使用烷化剂的患者相比,先使用烷化剂后未使用贝伐单抗的患者具有 PRS-1 的优势。MGMT 启动子甲基化和年龄与 PRS-1 预后相关。还对模型 1 和模型 2 进行了多变量分析,以了解具有已知 IDH 状态的患者亚群并排除患有 IDH 突变肿瘤的患者。MGMT 时的 HR 为 0.57,这证实了 PRS-1 在首次复发时接受烷化剂与贝伐单抗的患者的预后意义。病情和年龄没有预后。对于先接受烷化剂的患者和先接受贝伐单抗的患者,PRS-1 在第一次复发时均优于接受烷化剂的患者,对于任何进一步复发的患者,与第一次复发使用贝伐单抗然后使用烷化剂相比,对于烷化剂的比较,不先使用贝伐单抗,先使用贝伐单抗,然后在复发时不使用烷化剂。与该亚组的模型 1 相比,MGMT 状态和年龄不是重要的预后因素。
本研究检查了胶质母细胞瘤患者在首次复发时接受烷基化化疗或贝伐单抗治疗的结果,按 MGMT 启动子甲基化状态分层,然后进行补救治疗。在全球范围内,对于胶质母细胞瘤首次复发的护理标准尚未达成共识。在药物治疗方面,贝伐单抗在美国和其他一些国家没有被批准用于治疗复发性胶质母细胞瘤。在欧洲,烷化剂治疗已被广泛接受用于复发性胶质母细胞瘤患者,尤其是因为贝伐单抗的使用受到限制。因此,在几项随机 III 期试验中,洛莫司汀被选为实验药物的比较剂。胶质母细胞瘤复发时选择烷基化化疗或贝伐单抗治疗也可能取决于 MGMT 启动子甲基化状态,因为试验表明 TMZ 治疗与 TmmG 治疗的 MGMT 启动子患者相比 MGMT 启动子甲基化肿瘤患者的预后 -未甲基化的肿瘤要好得多。尽管阶段试验表明,与单独使用洛莫司汀相比,贝伐单抗和洛莫司汀联合治疗对 OS 没有益处,但贝伐单抗延长无进展生存期仍被认为是有益的,尤其是在肿瘤相关症状负担方面。总之,烷基化化疗或贝伐单抗是否应作为首次复发时的首选治疗方案仍存在争议。正如试验表明,TMZ 治疗与 TmmG 治疗的具有 MGMT 启动子的患者相比,具有 MGMT 启动子甲基化-未甲基化肿瘤的患者的预后要好得多。尽管阶段试验表明,与单独使用洛莫司汀相比,贝伐单抗和洛莫司汀联合治疗对 OS 没有益处,但贝伐单抗延长无进展生存期仍被认为是有益的,尤其是在肿瘤相关症状负担方面。总之,烷基化化疗或贝伐单抗是否应作为首次复发时的首选治疗方案仍存在争议。正如试验表明,TMZ 治疗与 TmmG 治疗的具有 MGMT 启动子的患者相比,具有 MGMT 启动子甲基化-未甲基化肿瘤的患者的预后要好得多。尽管阶段试验表明,与单独使用洛莫司汀相比,贝伐单抗和洛莫司汀联合治疗对 OS 没有益处,但贝伐单抗延长无进展生存期仍被认为是有益的,尤其是在肿瘤相关症状负担方面。总之,烷基化化疗或贝伐单抗是否应作为首次复发时的首选治疗方案仍存在争议。尽管阶段试验表明,与单独使用洛莫司汀相比,贝伐单抗和洛莫司汀联合治疗对 OS 没有益处,但贝伐单抗延长无进展生存期仍被认为是有益的,尤其是在肿瘤相关症状负担方面。总之,烷基化化疗或贝伐单抗是否应作为首次复发时的首选治疗方案仍存在争议。尽管阶段试验表明,与单独使用洛莫司汀相比,贝伐单抗和洛莫司汀联合治疗对 OS 没有益处,但贝伐单抗延长无进展生存期仍被认为是有益的,尤其是在肿瘤相关症状负担方面。总之,烷基化化疗或贝伐单抗是否应作为首次复发时的首选治疗方案仍存在争议。
分析支持在首次复发时选择烷基化化疗和贝伐单抗进行延迟治疗,因为与贝伐单抗相比,首次复发时接受烷基化化疗的患者 PRS-1 更长,多变量分析的 HR 为 0.59。由于 MGMT 启动子甲基化和年龄是多变量分析中 PRS-1 的重要预后因素,预后因素的差异可能有助于报告的结果数据。值得注意的是,无论 MGMT 启动子甲基化状态如何,接受烷基化化疗的患者的 PRS-1 都比接受贝伐单抗的患者长。鉴于 MGMT 启动子未甲基化肿瘤患者的预后较差,并且在已知 IDH 状态的亚群中接受贝伐单抗或烷化剂治疗的患者组之间 PRS-1 缺乏差异,排除 IDH 突变的肿瘤患者对于 MGMT 启动子未甲基化胶质母细胞瘤患者的任何补救治疗的使用是有问题的。迄今为止,没有数据比较烷化剂或贝伐单抗与最佳支持治疗,尤其是在 MGMT 患者组中具有未甲基化启动子的胶质母细胞瘤中。来自 3 期试验的数据表明,具有 MGMT 启动子甲基化的复发性胶质母细胞瘤患者接受了贝伐单抗,但没有接受具有更长 OS 的洛莫司汀。然而,这并未在一项临床试验中得到证实,该试验显示 MGMT 启动子甲基化的预后作用与患者接受洛莫司汀联合贝伐单抗或单独贝伐单抗无关。关于 MGMT 价值的结论 然而,由于本试验中没有不含洛莫司汀的治疗组,洛莫司汀的可用性和有效性是有限的。总之,贝伐单抗的存在不支持 MGMT 启动子甲基化的存在或不存在,而烷基化化疗可能对复发性胶质母细胞瘤和甲基化 MGMT 启动子的患者有益。

关于首次烷化剂或贝伐单抗治疗后进一步挽救治疗的效果,发现使用烷化剂后贝伐单抗比较 PRS-1 和 PRS-2 的时间更长。对这些数据的解释受到治疗医师的潜在选择偏倚、预后因素的差异和抢救治疗的异质性的限制,包括患者在任何进一步的复发治疗中被分组接受烷化剂或贝伐单抗,而没有进一步的复发分层将进一步限制每个子组的样本量。然而,在一项将 MGMT 启动子甲基化和年龄作为预后辅助因素的多变量分析中,证实了与首次使用贝伐单抗治疗的患者相比,使用烷基化药物治疗的患者具有更有利的结果。尽管如此,在对不同交叉方案的多变量分析中,与贝伐单抗优先方案的患者相比,烷化剂和含贝伐单抗方案的患者比贝伐单抗优先方案的患者具有 PRS-1 优势。,然后仅用于具有已知 IDH 状态的亚组和随后确认有烷化剂的患者。具有 IDH 突变的患者被排除在外,而不是整个患者队列。
一项流行病学研究表明,早期使用贝伐单抗治疗复发性胶质母细胞瘤可能没有益处,流行病学研究支持这一发现,表明在初次复发时未接受贝伐单抗治疗的患者没有益处。PRS 比接受该药物作为复发疾病首选药物的患者要长。一项对 298 例复发性胶质母细胞瘤患者的回顾性分析发现,在早期和延迟贝伐单抗给药之间,开始使用贝伐单抗的患者进一步肿瘤进展的中位时间没有显着差异。然而,延迟接受贝伐单抗治疗的患者中位 OS 更长。后一项研究中的 OS 益处可以通过选择偏倚和预后因素来解释,但也可能表明受益于其他疗法,包括用于复发性胶质母细胞瘤的早期烷化剂。另一项对 468 名因不同胶质母细胞瘤复发而接受贝伐单抗治疗的患者进行的回顾性研究未发现显着差异,无论是在进一步肿瘤进展的时间上,还是在贝伐单抗开始后的存活率上。该试验最初是作为 II 期试验开始的,包括贝伐单抗和洛莫司汀单药治疗,有可能跨越进一步复发。发表在 中的试验早期阶段的结果表明,治疗组的中位 OS 相似。然而,最终结果可能为确定复发性胶质母细胞瘤中烷基化化疗或贝伐单抗的顺序提供进一步的证据。另一项对 468 名因不同胶质母细胞瘤复发而接受贝伐单抗治疗的患者进行的回顾性研究未发现显着差异,无论是在进一步肿瘤进展的时间上,还是在贝伐单抗开始后的生存期上。该试验最初是作为 II 期试验开始的,包括贝伐单抗和洛莫司汀单药治疗,有可能跨越进一步复发。发表在 中的试验早期阶段的结果表明,治疗组的中位 OS 相似。然而,最终结果可能为确定复发性胶质母细胞瘤中烷基化化疗或贝伐单抗的顺序提供进一步的证据。另一项对 468 名因不同胶质母细胞瘤复发而接受贝伐单抗治疗的患者进行的回顾性研究未发现显着差异,无论是在进一步肿瘤进展的时间上,还是在贝伐单抗开始后的生存期上。该试验最初是作为 II 期试验开始的,包括贝伐单抗和洛莫司汀单药治疗,有可能跨越进一步复发。发表在 中的试验早期阶段的结果表明,治疗组的中位 OS 相似。然而,最终结果可能为确定复发性胶质母细胞瘤中烷基化化疗或贝伐单抗的顺序提供进一步的证据。该试验最初是作为 II 期试验开始的,包括贝伐单抗和洛莫司汀单药治疗,有可能跨越进一步复发。发表在 中的试验早期阶段的结果表明,治疗组的中位 OS 相似。然而,最终结果可能为确定复发性胶质母细胞瘤中烷基化化疗或贝伐单抗的顺序提供进一步的证据。该试验最初是作为 II 期试验开始的,包括贝伐单抗和洛莫司汀单药治疗,有可能跨越进一步复发。发表在 中的试验早期阶段的结果表明,治疗组的中位 OS 相似。然而,最终结果可能为确定复发性胶质母细胞瘤中烷基化化疗或贝伐单抗的顺序提供进一步的证据。
鉴于队列和上述研究中使用贝伐单抗治疗的患者预后不良,其在复发性胶质母细胞瘤患者中的应用仍然值得怀疑。症状控制仍然是主要症状之一。在再次照射的情况下,据报道,当共同暴露于贝伐单抗时,有症状的患者出现症状性放射性坏死和水肿,辐射相关毒性降低。然而,由于缺乏前瞻性随机研究,对复发性胶质母细胞瘤患者单独或联合贝伐单抗进行再照射的价值仍存在争议。一项对 71 名患者的回顾性研究表明,PFS 和 OS 可能具有一定的潜在益处,而另一项针对 14 名患者的小型队列研究显示,复发性“高级别”胶质瘤患者的 PFS 更高,但通过使用和不使用贝伐单抗进行再照射可以缩短 OS。在一项 1 期临床试验中,对 15 名患者进行了前瞻性评估,联合再照射和贝伐单抗,剂量增加至 3×11 Gy,中位总生存期为 13 个月。除了已经讨论的研究局限性之外,由于患者队列的异质性和亚组中的少数患者,该分析的回顾性也限制了数据解释。总之,本研究证实贝伐单抗在复发性胶质母细胞瘤中的价值在生存方面是有限的,并且结果与 MGMT 状态无关。烷化剂在复发性胶质母细胞瘤患者中具有活性,主要是在甲基化 MGMT 启动子的情况下。在一项 1 期临床试验中,对 15 名患者进行了前瞻性评估,联合再照射和贝伐单抗,剂量增加至 3×11 Gy,中位总生存期为 13 个月。除了已经讨论的研究局限性之外,由于患者队列的异质性和亚组中的少数患者,该分析的回顾性也限制了数据解释。总之,本研究证实贝伐单抗在复发性胶质母细胞瘤中的价值在生存方面是有限的,并且结果与 MGMT 状态无关。烷化剂在复发性胶质母细胞瘤患者中具有活性,主要是在甲基化 MGMT 启动子的情况下。在一项 1 期临床试验中,对 15 名患者进行了前瞻性评估,联合再照射和贝伐单抗,剂量增加至 3×11 Gy,中位总生存期为 13 个月。除了已经讨论的研究局限性之外,由于患者队列的异质性和亚组中的少数患者,该分析的回顾性也限制了数据解释。总之,本研究证实贝伐单抗在复发性胶质母细胞瘤中的价值在生存方面是有限的,并且结果与 MGMT 状态无关。烷化剂在复发性胶质母细胞瘤患者中具有活性,主要是在甲基化 MGMT 启动子的情况下。15 名患者接受了再照射和贝伐单抗联合治疗的前瞻性评估,剂量增加至 3 × 11 Gy,中位总生存期为 13 个月。除了已经讨论的研究局限性之外,由于患者队列的异质性和亚组中的少数患者,该分析的回顾性也限制了数据解释。总之,本研究证实贝伐单抗在复发性胶质母细胞瘤中的价值在生存方面是有限的,并且结果与 MGMT 状态无关。烷化剂在复发性胶质母细胞瘤患者中具有活性,主要是在甲基化 MGMT 启动子的情况下。15 名患者接受了再照射和贝伐单抗联合治疗的前瞻性评估,剂量增加至 3 × 11 Gy,中位总生存期为 13 个月。除了已经讨论的研究局限性之外,由于患者队列的异质性和亚组中的少数患者,该分析的回顾性也限制了数据解释。总之,本研究证实贝伐单抗在复发性胶质母细胞瘤中的价值在生存方面是有限的,并且结果与 MGMT 状态无关。烷化剂在复发性胶质母细胞瘤患者中具有活性,主要是在甲基化 MGMT 启动子的情况下。众所周知,由于患者队列的异质性和亚组中的少数患者,分析的回顾性也限制了数据解释。总之,本研究证实贝伐单抗在复发性胶质母细胞瘤中的价值在生存方面是有限的,并且结果与 MGMT 状态无关。烷化剂在复发性胶质母细胞瘤患者中具有活性,主要是在甲基化 MGMT 启动子的情况下。众所周知,由于患者队列的异质性和亚组中的少数患者,分析的回顾性也限制了数据解释。总之,本研究证实贝伐单抗在复发性胶质母细胞瘤中的价值在生存方面是有限的,并且结果与 MGMT 状态无关。烷化剂在复发性胶质母细胞瘤患者中具有活性,主要是在甲基化 MGMT 启动子的情况下。
威海链 » DNA修复基因的启动子甲基化06-甲基鸟嘌呤DNA甲基成立
免责声明:本文由提供互联网分享,不代表本网的观点和立场;如有侵权请联系删除。
